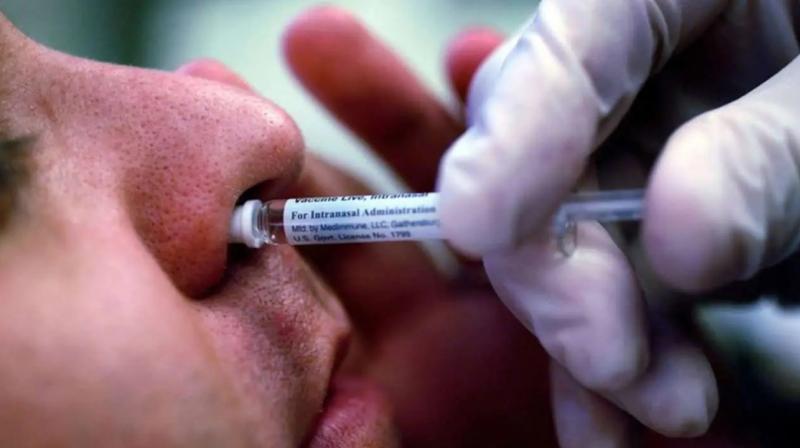
नई दिल्ली: ड्रग कंट्रोलर जनरल ऑफ इंडिया ने भारत बायोटेक को इंट्रानैसल कोविड बूस्टर खुराक के टेस्टिंग के लिए अपनी मंजूरी दे दी है। यह ट्रायल 900 लोगों पर किया जाएगा। डीसीजीआई की विषय विशेषज्ञ समिति (SEC) ने भारत बायोटेक को अपने इंट्रानैसल कोविड वैक्सीन के लिए ‘चरण- III बूस्टर खुराक अध्ययन’ के लिए ‘सैद्धांतिक’ मंजूरी दी, जो भारत में अपनी तरह का पहला है और इसे तीन सप्ताह पहले अनुमोदन के लिए प्रोटोकॉल जमा करने के लिए कहा है।
भारत बायोटेक ने देश में टीकाकरण के लिए कोविडशील्ड, कोवैक्सीन और स्पूतनिक वी को मंजूरी दे दी है। कोवैक्सीन को DCGI की 28-दिवसीय बहु-खुराक शीशी नीति (MDVP) और WHO आपातकालीन उपयोग सूची (WHO EUL) के तहत उपयोग के लिए अप्रूव किया गया है।
आपको बता दें कि अब जल्द ही बाजारों में भी ये टीका आसानी से उपलब्ध होगा क्योंकि आज यानी गुरुवार को ड्रग कंट्रोलर जनरल ऑफ इंडिया (डीसीजीआई) ने इसे सशर्त मंजूरी दे दी है। इस संबंध में और अधिक जानकारी देते हुए केंद्रीय स्वास्थ्य मंत्री डॉ मनसुख मंडाविया ने बताया कि केंद्रीय औषधि मानक नियंत्रण संगठन (सीडीएससीओ) ने अब कोवैक्सिन और कोविशील्ड को मिली आपातकालीन स्थितियों में उपयोग की मंजूरी को अपग्रेड करते हुए वयस्क आबादी में कुछ शर्तों के साथ सामान्य नई दवा के रूप में इस्तेमाल को मंजूरी दे दी है। डीसीजीआई तय की गई शर्तों के मुताबिक, दोनों वैक्सीन दुकानों पर नहीं मिलेगी। प्राइवेट अस्पतालों और क्लिनिक ही टीके खरीद सकेंगे तथा वहीं लगाई।
Top Hindi News, Latest News Updates, Delhi Updates,Haryana News, click on Delhi Facebook, Delhi twitter and Also Haryana Facebook, Haryana Twitter.